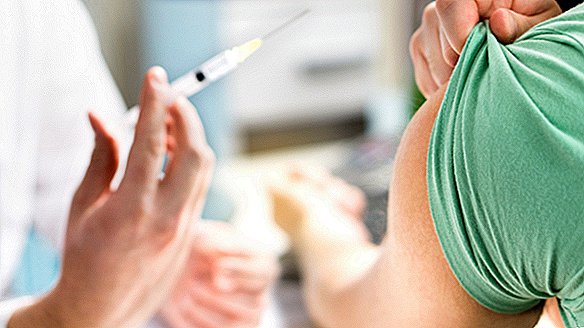
Здоровий доброволець у Сіетлі - перша людина в США, яка отримала дозу експериментальної коронавірусної вакцини у рамках нового клінічного випробування, повідомили сьогодні (16 березня) урядові службовці охорони здоров'я.
Протягом наступних шести тижнів дослідники планують зарахувати 45 учасників випробування, які перевірять безпеку вакцини, а також її здатність викликати імунну відповідь у добровольців. Випробування відбудеться у Вашингтонському науково-дослідному інституті охорони здоров’я Kaiser Permanente (KPWHRI) у Сіетлі.
Національний інститут алергії та інфекційних хвороб (NIAID) дозволив новій вакцині швидко простежити клінічні випробування без ретельного тестування на моделях на тваринах, що, як правило, є суворою передумовою тестування на людях. Хоча перехід до випробувань на людях може принести вакцину на ринок швидше, це лише перший крок.
Нові препарати повинні пройти три ітераційні етапи клінічних випробувань, перш ніж вони будуть визнані безпечними та ефективними для широкого застосування. Якщо припустити, що початкові випробування пройдуть добре, це може пройти за 12 до 18 місяців, перш ніж будь-яка вакцина буде готова до загального користування, заявив директор БНІАД Ентоні Фочі 12 березня.
"Пошук безпечної та ефективної вакцини для запобігання зараження SARS-CoV-2 є невідкладним пріоритетом для охорони здоров'я", - заявив Фокі в заяві NIAID, опублікованій 16 березня. крок до досягнення цієї мети ".
Нова вакцина - це співпраця між вченими NIAID та біотехнологічною компанією Moderna Inc., що базується в Кембриджі, штат Массачусетс.
Коронавірусна наука та новини
-Коронавірус у США: карта та випадки
-Які симптоми?-Наскільки смертельно небезпечний новий коронавірус?-Як довго вірус тримається на поверхні?-Чи є ліки від COVID-19?-Як вона порівнюється із сезонним грипом?-Як поширюється коронавірус?-Чи можуть люди поширити коронавірус після одужання?
Що таке випробування "Фаза 1"?
Випробування, розпочате сьогодні, відоме як "клінічне випробування фази 1", тобто його основна мета полягає в наданні інформації про те, як вакцина взаємодіє зі здоровим організмом людини, згідно з даними американського управління харчових продуктів та лікарських препаратів (FDA).
Випробування фази 1 обстежують невелику групу людей, як правило, від 20 до 80 осіб, які отримують різні дози експериментального лікування. Протягом кількох місяців дослідники стежать за тим, як кожен доброволець метаболізує дане лікування та які загальні побічні ефекти виникають у відповідь на різні дози. 45 добровольців у новому випробуванні отримуватимуть різні дози нової вакцини, що називається мРНК-1273, і будуть контролюватися протягом 14-місячного періоду. Волонтери отримають дві ін'єкції вакцини у верхню частину руки, з 28-денним розривом між дозами.
Перший учасник отримає найнижчу дозу вакцини - 25 мкг (мкг) на ін'єкцію, згідно з заявою NIAID. Три інші отримають таку саму початкову дозу, а ще чотири отримають 100-мг дозу вакцини і будуть ретельно оцінені перед тим, як будь-яким добровольцям буде надано другу дозу. Якщо реакції учасників на низькі дози виявляться прийнятними, третя група учасників отримуватиме 250 мкг вакцини за ін'єкцію.
Крім моніторингу побічних ефектів, дослідники перевірять, чи викликає вакцина імунну відповідь, аналізуючи кров добровольців на антитіла, повідомляє ClinicalTrials.gov.
Якщо вакцина працює як розроблено, імунна система повинна генерувати антитіла, які захоплюють характерний білок, виявлений на поверхні нового коронавірусу SARS-CoV-2, згідно з повідомленням Kaiser Permanente, медичної компанії, яка проводила дослідження. Замість того, щоб впроваджувати в організм мертвий або ослаблений вірус, щоб викликати цю реакцію, як це роблять звичайні вакцини, вакцина доручає клітинам самі будувати вірусний білок, використовуючи молекулу, яку називають месенджерою РНК (мРНК). Після використання організмом мРНК повинна руйнуватися і ліквідуватися, залишаючи позаду лише захисні антитіла.
Наступні кроки
Випробування фази 2 зазвичай вивчають кілька сотень людей та стежать за учасниками протягом періодів від декількох місяців до двох років. Перш за все, випробування фази 2 служать вторинним заходом безпеки і допомагають дослідникам уточнити дозування певного препарату. На цьому етапі дослідники відбирають учасників з такими ознаками, як вік та фізичне здоров'я, які відповідають тим людям, для яких вакцина розробляється. (Наприклад, хоча будь-хто може заразитись COVID-19, ті, хто має похилий вік, і ті, хто має хронічні стани, мають більшу ймовірність розвитку важких симптомів, тому це може бути врахуванням у фазах 2 випробувань.)
Випробування фази 3 зазвичай тривають від 300 до 3000 добровольців протягом одного-чотирьох років, згідно з FDA. З більшою групою людей дослідники можуть відзначити незвичайні побічні ефекти препарату, і, подовжуючи період дослідження, вони можуть вловлювати довгострокові побічні ефекти по мірі їх появи. Фаза 3 випробувань повинна продемонструвати, що даний препарат забезпечує ті медичні переваги, які він призначений; якщо ця коронавірусна вакцина пройде цей тест, FDA може схвалити препарат для широкого застосування.
Ця коронавірусна вакцина може або не може досягти випробувань фази 4 у найближчі роки, хоча поки що обмежені дослідження на мишах показали багатообіцяючі результати. Тим часом дослідницькі групи по всьому світу продовжуватимуть розробляти альтернативні вакцини для боротьби з розповсюдженням COVID-19, повідомляє The Associated Press.