Давно відомо, що всі молекули мають два рівні і протилежні заряди, які розділені на певній відстані. У випадку таких полярних молекул центр негативного заряду не збігається з центром позитивного заряду. Ступінь полярності в таких ковалентних молекулах може бути описана терміном "Дипольний момент", який по суті є мірою полярності в полярній ковалентній зв'язку.
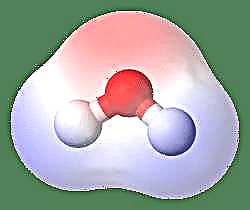
Найпростіший приклад диполя - молекула води. Молекула води полярна через нерівномірний розподіл її електронів у «зігнутій» структурі. Молекула води утворює кут, з атомами водню на верхівках і киснем у вершині. Оскільки кисень має більшу електронегативність, ніж водень, сторона молекули з атомом кисню має частковий негативний заряд, тоді як водень у центрі має частковий позитивний заряд. Через це напрям дипольного моменту вказує на кисень.
Мовою фізики, електричний дипольний момент - це міра поділу позитивних та негативних електричних зарядів у системі зарядів, тобто міра загальної полярності системи зарядів - тобто розділення електричного заряду молекул, який призводить до диполя. Математично і у простому випадку двох точкових зарядів, одного із зарядом + q та одного із зарядом? Q, електричний дипольний момент p може бути виражений як: p = qd, де d - вектор переміщення, що вказує від негативного заряду до позитивний заряд. Таким чином, вектор електричного дипольного моменту p вказує від негативного заряду до позитивного заряду.
Інший спосіб поглянути на це - зобразити Дипольний Момент грецькою літерою m, m = ed, де e - електричний заряд, d - відстань поділу. Він виражається в одиницях Debye і записується як D (де 1 Debye = 1 x 10-18e.s.u см). Дипольний момент є векторною величиною і тому представлений невеликою стрілкою з хвостиком у позитивному центрі та головою, що спрямована до негативного центру. У випадку молекули води момент диполя становить 1,85 D, тоді як молекула соляної кислоти 1,03 D і може бути представлена як:
Ми написали багато статей про дипольний момент для Space Magazine. Ось стаття про те, з чого складається вода, і ось стаття про молекули.
Якщо вам потрібна додаткова інформація про дипольний момент, перегляньте ці статті з «Гіперфізики та науки щодня».
Ми також записали цілий епізод Астрономічної ролі про молекули в космосі. Слухайте тут, Епізод 116: Молекули в космосі.
Джерела:
http://en.wikipedia.org/wiki/Electric_dipole_moment
http://en.wikipedia.org/wiki/Dipole
http://www.tutorvista.com/content/chemistry/chemistry-iii/chemical-bonding/degree-polarity.php
http://hyperphysics.phy-astr.gsu.edu/hbase/electric/dipole.html#c1
http://en.wikipedia.org/wiki/Water_molecule